锂离子电池(LIB)是一种非常有前景的储能系统选择,可通过为电动汽车(EV)提供动力以及将清洁但间歇性的能源整合到电网中来最大程度地减少对化石燃料的依赖。然而,传统电池正在遭受损失由于传统锂离子电池中使用的可燃液态电解质引起的安全问题。然而,全固态电池(ASSB)成为最有前景的技术之一,因为它们可能提供更好的安全性、更高的能量密度和更长的循环寿命与基于液态电解质的电池相比。使用固态电解质(SE)作为液态电解质的替代品提供了使用高压正极和金属负极的可能性,有助于实现高理论能量密度(体积能量密度为500−700Wh/L,重量能量密度为300−500Wh/kg)。
固态电解质是ASSB中最重要的组成部分,因为它在很大程度上决定了功率密度和倍率性能。ASSB面临的一个主要挑战是开发高导电性SE(>1 mS cm−1)以及良好的电化学稳定性。这激发了在寻找能够与流动性同行竞争的新社会企业方面付出了巨大的努力。大量的工作使人们对SE中的离子传输机制有了深入的了解,并显著提高了离子电导率。在众多广泛研究的SE候选材料中,硫化物表现出最高的电导率,高达10−2S cm−1,其中一些甚至超过了液态电解质的值。例子包括Li10GeP2S12(“LGPS”;σi=12 mS·cm−1)及其衍生物,Li7P3S11(σi=17 mS·cm−1),Li argyrodite Li6PS5X(X=Cl,Br)(σi=3−7 mS·cm−1)和Li9.54Si1.74P1.44S11.7Cl0.3(σi=25 mS·cm−1)。然而,硫化物通常表现出较窄的电化学窗口,因此与锂金属负极的兼容性较差。此外,硫化物在潮湿空气中极高的敏感性很大程度上阻碍了它们在电池中的实际应用。另一方面,氧化物电解质通常表现出高氧化电位和良好的化学/电化学稳定性,但延展性较差,而且与正极接触时界面电阻大。非常需要开发同时具有高离子电导率、良好机械性能和宽电化学窗口的SE。
基于卤化物的电解质只受到了适度的关注,很少有材料被报道为锂离子导体,第一个例子可以追溯到1950年代。2018年,Asano等人显著提高了卤化物的室温电导率(Li3YCl6为0.51 mS cm-1,Li3YBr6为1.7 mS cm−1)。值得注意的是,这些材料在良好的电化学稳定性、机械变形性以及在没有保护层的情况下与典型正极材料的优异相容性方面展示了其作为SE材料的优势。从那时起,人们对三元卤化物的兴趣高涨,因为它们与高压正极接触时具有高抗氧化性。几种三元卤化物Li3YCl6,30Li3ErCl6,Li3InCl6,LixScCl3+x,Li2ZrCl6,0.5LiCl·SmCl3,LiMCl6(M=Ta,Nb)及其异价取代变体Li3−xM1−xZrxCl6(M=Y,Er,In,Ho,Lu),Li3−xYb1−xMxCl6(M=Hf4+,Zr4+),LiMOCl4(M=Nb,Ta),ZrO2(-LiCl)-Li2ZrCl6,Li2+x-yZrCl6-x-yOx,xLi2OMCly(M=Ta,Hf),已(重新)研究。用四价阳离子异价取代M3+导致电导率增加几个数量级。几种组合物在室温下实现了高达几mS cm−1的高电导率,但潜在的离子传导机制仍然难以捉摸。以往影响锂导电卤化物离子输运因素的研究主要集中在非锂阳离子无序、多面体畸变、堆垛层错等方面,而Li/空位浓度对离子的影响传输机制和离子传输特性尚未详细阐明。
中科院物理所吴凡团队、胡勇胜团队和中山大学章志珍团队合作,报导了新型锂超离子氯化物Li3−xSc1−xZrxCl6和Li3−xSc1−xHfxCl6(x=0.25,0.50,0.625,0.75),它们在室温下表现出高达2.2 mS cm−1的高离子电导率以及低电导率活化能垒(Zr和Hf类比分别为0.31和0.33eV)。Zr4+/Hf4+取代后电导率的显著提高归因于沿c轴的能垒降低以及由调整的Li+/空位浓度引起的相关迁移的增强。固态电池的评估进一步证实了该电解质在高压ASSB中的应用潜力。工作阐明了调整阳离子/空位浓度的影响,从而增强了相关迁移对阳离子电导率的影响。该策略可以扩展到其他系统,并作为快离子导体设计的指南。该研究以“Superionic Conductivity Invoked by Enhanced Correlation Migration in Lithium Halides Solid Electrolytes”为题,发表在储能领域著名期刊《ACS Energy Letters》上(IF=22)。
使用包含球磨的固态合成工艺分别合成了分子式为Li3−xSc1−xZrxCl6和Li3−xSc1−xHfxCl6(x=0,0.25,0.50,0.625,0.75)的Zr和Hf取代的Li3ScCl6以及后续的退火工艺。通过X射线衍射仪对所制备的产物的晶体结构进行了表征。Li3−xSc1−xZrxCl6和Li3−xSc1−xHfxCl6(x=0,0.25,0.50,0.625,0.75,1.0)的XRD图案分别如图1a所示。注意到端元Li3ScCl6和Li2ZrCl6(或Li2HfCl6)均以单斜晶结构结晶,空间群为C2/m,因此在XRD图案中显示出相同的hkl线。两个端元之间的峰相对强度的差异是由于Li含量的差异、不同的威科夫位点以及Sc/Zr原子的占据而引起的。由于Sc3+(74.5pm)和Zr4+(72.0pm)或Hf4+(71.0pm)之间的离子半径接近,当x在0和1之间变化时,形成固溶体。先前的Rietveld针对单晶X射线衍射数据进行了精修Li3ScCl6识别出锂原子的三个不同的威科夫位点,即Li1(4g)、Li2(4h)和Li3(2d),其中Li2和Li3位点被部分占据,而Li1位点被完全占据。与X射线相比考虑到氧化锆、铪、钪和氯化物具有较大的正中子散射长度(Zr、Hf,Sc和Cl分别为b=7.2、7.7、12.3和9.6fm),中子衍射预计在确定锂无序原子占据方面会更加准确),而锂是负值(b=-1.9fm),这提供了大的散射对比度。因此,对合成的化合物Li3−xSc1−xZrxCl6(x=0,0.25,0.625,0.75)进行了中子粉末衍射。从单晶XRD确定的模型被用作改进的起点。骨架原子(Sc/Zr、Cl)的坐标与文献没有太大差异。值得注意的是,测试表明,具有三个部分占据的锂位点的模型与NPD数据产生了最佳的一致性,这与单晶XRD形成鲜明对比,其中Li1位点被细化为完全占据。BVSE方法的位点能量分析表明不存在高能位点,并且三个Li位点具有非常相似的位点能量,这将在下面证明。图1b显示了Li2.375Sc0.375Zr0.625Cl6在室温下测量的中子衍射数据的Rietveld细化图案。拟合结果令人满意,所有原子的原子位置和原子位移参数都得到了精确的修正。还对所有组合物的XRD图案进行了细化,目的是获得更全面的信息。Zr取代后晶格参数的变化如图1c所示。相应细化的3D框架如图1d−f所示。Zr取代后,a轴和c轴的晶格参数分别随x表现出单调增加和减少的趋势。相反,b轴随着x的增大先增大后减小,在x=0.625时获得最大值。下面将讨论这些结构变化对Li+离子扩散性能的影响。
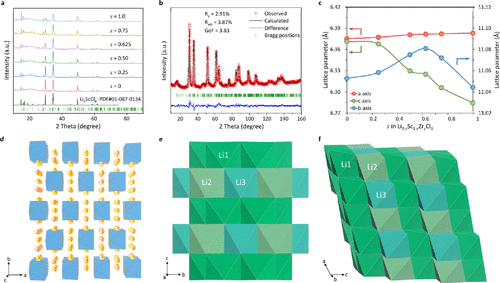
【图1】(a)使用Cu源的Li3−xSc1−xZrxCl6(x=0,0.25,0.50,0.625,0.75,1.0)的粉末X射线衍射图。(b)Li2.375Sc0.375Zr0.625Cl6在室温下的中子粉末衍射图和相应的Rietveld精修。红圈是实验数据。黑线表示计算出的模式。蓝色曲线是差异图,深绿色垂直刻度代表布拉格反射。(c)Li3−xSc1−xZrxCl6的晶格参数作为Zr4+(x)量的函数。(d)Li3−xSc1−xZrxCl6的晶体结构沿[001]方向显示。(Sc/Zr)Cl6八面体显示为蓝色,Li+离子显示为金色球体。(e,f)LiCl6八面体的排列(e)沿[100]方向和(f)沿[010]方向。深绿色、水绿色和青色的八面体分别对应于Li1、Li2和Li3。
通过交流阻抗谱(IS)测量Li3−xSc1−xZrxCl6和Li3−xSc1−xHfxCl6(x=0、0.25、0.50、0.625、0.75和1.0)压制颗粒的离子传输行为,温度范围为298至333K(图2a-d)。图2a和图2c分别显示了Li3−xSc1−xZrxCl6和Li3−xSc1−xHfxCl6(x=0,0.25,0.50,0.625,0.75,1.0)的奈奎斯特图。低频区的线性Warburg元件是纯离子导体的典型特征。Li3−xSc1−xZrxCl6和Li3−xSc1−xHfxCl6(x=0,0.25,0.50,0.625,0.75,1.0)相应的室温(298K)离子电导率和活化能,由线性拟合确定总结了阿累尼乌斯图。随着x的增加,电导率首先增加至x=0.625,然后下降。下面讨论这一趋势背后的原因。注意到Li2ZrCl6和Li2HfCl6的电导率较低。25°C时为0.01 mS cm−1,与之前的文献非常一致。这些结果表明,通过异价取代调节锂/空位无序可提高离子电导率并降低活化能。两个版本的最高离子电导率(Zr类似物为2.2 mS cm−1,Hf类似物为1.1 mS cm−1)在x=0.625时实现。在导电性最高的组合物Li2.375Sc0.375Zr0.625Cl6和Li2.375Sc0.375Hf0.625Cl6中,Li+离子跳跃的总活化能分别为0.31和0.33eV。通过直流极化测量的Li2.375Sc0.375Zr0.625Cl6的电子电导率为3.1×10−10S cm−1,比离子电导率低7个数量级,表明其电子绝缘性质。
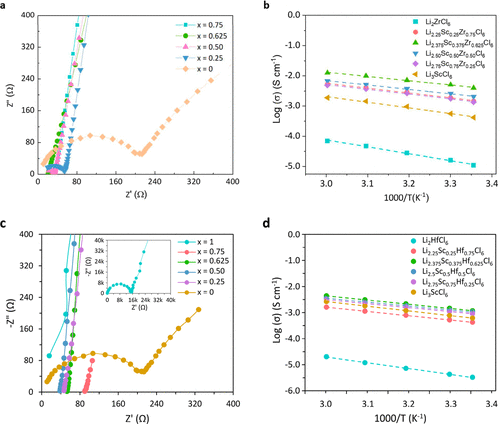
【图2】(a)Li3−xSc1−xZrxCl6(x=0,0.25,0.50,0.625,0.75)的阻抗谱。(b)Li3−xSc1−xZrxCl6(x=0,0.25,0.50,0.625,0.75,1.0)在不同温度(298−333K)下的Li+离子电导率。活化能由阿累尼乌斯图的斜率确定。(c)Li3−xSc1−xHfxCl6(x=0.25,0.50,0.625,0.75,1.0)的阻抗谱。(d)Li3−xSc1−xHfxCl6(x=0,0.25,0.50,0.625,0.75,1.0)在不同温度(298−333K)下的Li+离子电导率。虚线是数据的线性拟合,Li3ScCl6的活化能为0.44eV,Li2.75Sc0.75Zr0.25Cl6为0.36eV,Li2.50Sc0.50Zr0.50Cl6为0.33eV,Li2.375Sc0.375Zr0.625Cl6为0.31eV、Li2.25Sc0.25Zr0.75Cl6为0.34eV、Li2ZrCl6为0.47eV、Li2.75Sc0.75Hf0.25Cl6为0.35eV、Li2.50Sc0.50Hf0.50Cl6为0.34eV、Li2.375Sc0.375Hf0.625Cl6为0.33eV,Li2.25Sc0.25Hf0.75Cl6为0.36eV,Li2HfCl6为0.47eV。
为了探讨Zr/Hf取代对新合成化合物中Li+离子扩散倾向的影响,对Li3−xSc1−xMxCl6(M=Zr;x=0,0.25,0.625)进行了BVSE分析。Li3ScCl6和Li2.375Sc0.375Zr0.625Cl6在(010)和(001)方向投影的BVSE图分别如图3a和图3b所示。在两个系统中观察到沿c轴的连接性存在明显差异,如红色虚线所示。三种组合物的BVSE方法明确表明,与a或b轴相比,沿c轴的离子传输受到更高的能垒,这表明这些组合物中离子传输的瓶颈是由沿c轴的离子传输过程决定的。c轴。此外,Zr取代后沿c轴的Li+离子传输能垒降低(Li3ScCl6为0.59eV;Li2.75Sc0.75Zr0.25Cl6为0.55eV;Li2.375Sc0.375Zr0.625Cl6为0.52eV)(图3c−e)。为了揭示这种影响的根源,测量了锂离子传输的跳跃距离和瓶颈区域。Zr4+取代后沿c轴的跳跃距离缩短,因为晶格沿该方向收缩。值得注意的是,随着x的增加,Li+离子传输的三角形瓶颈面积也随之增加。这些导致Li+离子沿c方向跳跃的能垒降低(图3f)。注意到离子电导率同时由活化能(Ea)和载流子浓度(n)决定。这两个因子单调变化,但方向相反且变化率不同,导致相关性在x=0.625处达到最大值。AIMD模拟在650至950K的高温下进行,以加速扩散并缩短模拟时间。模拟过程中没有Zr/Hf−Cl或Sc−Cl键断裂,这证实了相稳定性。图3h显示了AIMD模拟中Li3−xSc1−xMxCl6(M=Zr/Hf;x=0,0.625)的Li+离子扩散系数的阿伦尼乌斯图。Li3−xSc1−xMxCl6(M=Zr/Hf;x=0.625)中的Li+离子扩散率远高于Li3ScCl6中的扩散率。此外,Li3ScCl6、Li2.375Sc0.375Zr0.625Cl6和Li2.375Sc0.375Hf0.625Cl6的拟合活化能分别为0.29、0.21和0.24eV。这些结果表明,用Zr/Hf替代Sc后,Li+离子扩散显著增强。
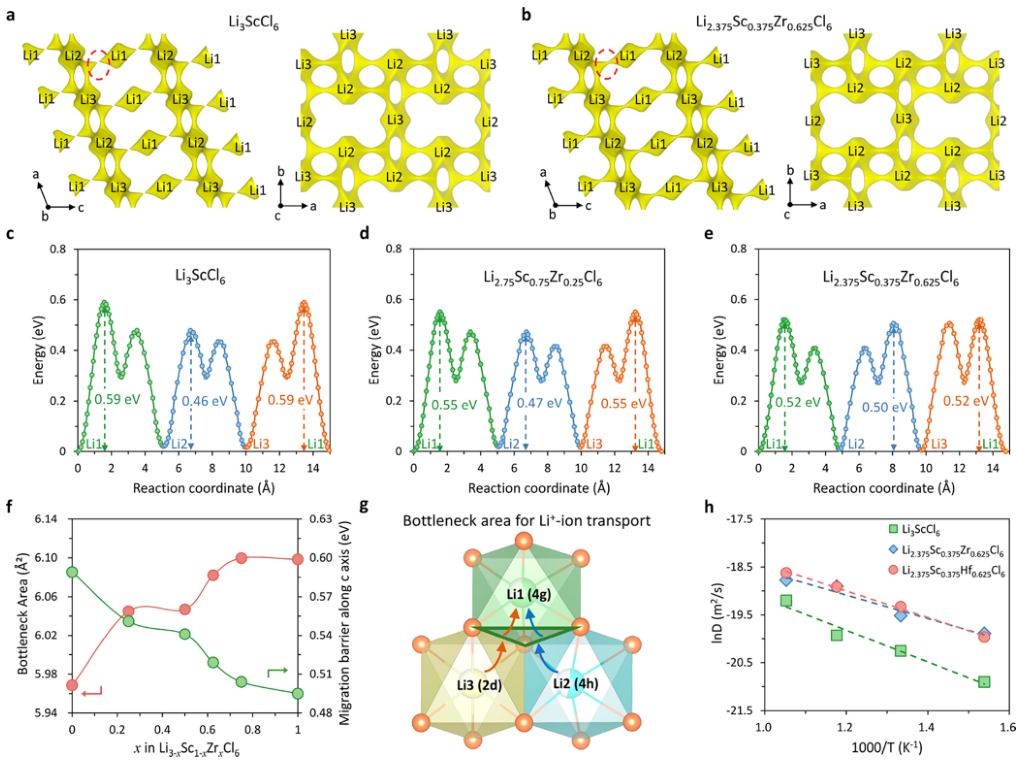
【图3】通过键价位能(BVSE)方法计算(a)Li3ScCl6和(b)Li2.375Sc0.375Zr0.625Cl6中Li+离子的等值面(黄色)。(c−e)针对(c)Li3ScCl6、(d)Li2.75Sc0.75Zr0.25Cl6和(e)Li2.375Sc0.375Zr0.625Cl6的精制结构,通过BVSE方法得出的Li+离子迁移势垒。Li1位点的位点能量以零为参考,这是能量最低的。绿色和橙色部分分别代表Li1−Li2路径和Li3−Li1沿c方向的迁移势垒;蓝色部分描绘了ab平面中沿Li2−Li3路径的迁移势垒。(f)Li+离子沿c方向传输的瓶颈区域(红色曲线)和迁移势垒(绿色曲线)。瓶颈区域由细化结构导出,而能垒则通过BVSE方法计算。(g)Li+离子沿c方向传输的瓶颈示意图。(h)根据AIMD模拟在不同温度(650、750、850和950K)下计算的Li+离子示踪扩散率。虚线是数据的线性拟合,Li3ScCl6的活化能为0.29eV,Li2.375Sc0.375Zr0.625Cl6的活化能为0.21eV,Li2.375Sc0.375Hf0.625Cl6的活化能为0.24eV。
为了阐明异价取代对微观Li+离子传导的影响,进一步计算了vanHove相关函数来研究母体组合物Li3ScCl6和掺杂组合物Li2.375Sc0.375M0.625Cl6(M=Zr/Hf)中Li+离子的相关迁移。vanHove相关函数的自(Gs)部分描述了时间Δt后Li+离子相对于其初始位置的距离。0到2.0Å之间的Gs峰值对最近的Li−Li距离有响应,在Li3ScCl6中该峰值在3ps内衰减,而对于Li2.375Sc0.375M0.625Cl6(M=Zr/Hf)。Gs图中最近的Li的衰减时间表示Li原子的扩散。Li2.375Sc0.375M0.625Cl6(M=Zr/Hf)的Gs衰减速度快得多,表明其Li+离子扩散动力学比Li3ScCl6快得多。另一方面,vanHove相关函数的不同(Gd)部分(图4a、b)反映了时间Δt后不同Li+离子相对于所选Li+离子的径向分布。Li2.375Sc0.375M0.625Cl6(M=Zr或Hf)中空出的Li位点很可能立即被另一个Li+离子占据,这证实了相关的迁移。高度相关的离子迁移和由此产生的快速离子交换速率,以及扩大的瓶颈尺寸,产生了优异的离子传导性能。
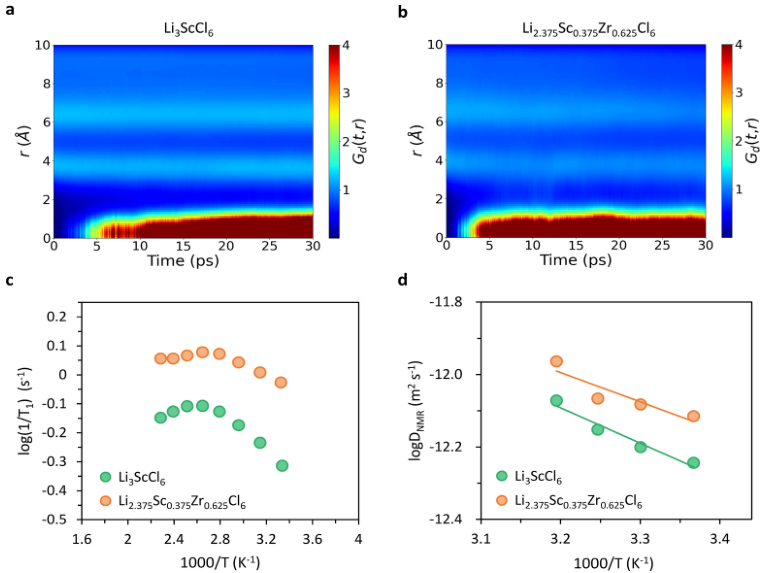
【图4】(a)Li3ScCl6和(b)Li2.375Sc0.375Zr0.625Cl6中范霍夫函数的独特部分。(c)Li3ScCl6和Li2.375Sc0.375Zr0.625Cl6在11.7T磁场下随温度变化的纵向7Li SLRNMR速率1/T1(log(1/T1)与1000/T作图)。(d)阿伦尼乌斯图Li3ScCl6和Li2.375Sc0.375Zr0.625Cl6的7Li扩散系数。
为了揭示异价取代对Li+离子传导的影响,通过采用时域7Li自旋晶格弛豫(SLR)NMR测量Li3ScCl6和Li2.375Sc0.375Zr0.625Cl6进一步探讨了Li+离子扩散动力学。SLR率(1/T1)与波动的局部场相关,并且可用于确定Li+离子相关时间τc。扩散引起的NMRSLR速率显示出特征温度Tmax,在该温度下Li+离子扩散过程的相关速率(1/τc)等于拉莫尔频率。也就是说,在峰值最大时,可以根据关系式ω0τc≈1来估计相关率。因此,在Tmax时,Li+离子扩散过程的相关时间可以计算为4.1×10−10s,拉莫尔频率为4.1×10−10s在测量中,7Li的频率为194MHz。在Li3ScCl6和Li2.375Sc0.375Zr0.625Cl6中,Tmax分别出现在约384和378K处(图4c),这意味着后者中Li+离子扩散过程的动力学更快。这与阻抗谱和AIMD模拟非常吻合。τc的温度依赖性在低温侧和高温侧分别遵循阿伦尼乌斯关系,根据该关系可以获得相关的活化能。不幸的是,由于数据统计有限,无法获得高温侧翼(长程锂离子扩散过程)活化能的合理拟合。进行Li脉冲场梯度核磁共振(PFG-NMR)测量以确定Li+离子示踪扩散系数。值得注意的是,在研究的温度范围(297−313K)内,Li2.375Sc0.375Zr0.625Cl6显示出比Li3ScCl6高得多的Li+离子示踪扩散系数(图4d)。温度相关扩散系数的线性拟合遵循阿伦尼乌斯关系。从相应的斜率确定Li2.375Sc0.375Zr0.625Cl6中Li+离子示踪剂扩散的活性能为0.16eV,低于Li3ScCl6(0.19eV)。
Li+离子的相关迁移可以通过Haven比(HR)来定量评估,它是示踪扩散系数(Dtracer)与宏观长程扩散系数(Dσ)的比值。Dσ可以从电导率推导出来根据Nernst−Einstein方程通过阻抗谱测量
![]()
其中n是移动离子的浓度。HR在0和1之间变化,较低的值对应于多个扩散跳跃之间的高相关性。与Li3ScCl6相比,Li2.375Sc0.375Zr0.625Cl6在所访问的温度范围内显示出低得多的HR,例如,在303K时为0.22 vs 0.71(表1)。这些结果表明,Zr取代的Li2.375Sc0.375Zr0.625Cl6中相关迁移的百分比要高得多。Li3ScCl6和Li2.375Sc0.375Zr0.625Cl6的HR值均随温度升高而下降,这意味着Li+离子扩散过程中的相关性跳跃更多。研究结果表明,调整的锂离子浓度和空位有助于增强此类固态电解质的相关迁移。Wagemaker小组之前的一项研究在β-Li3PS4中也报告了类似的观察结果。
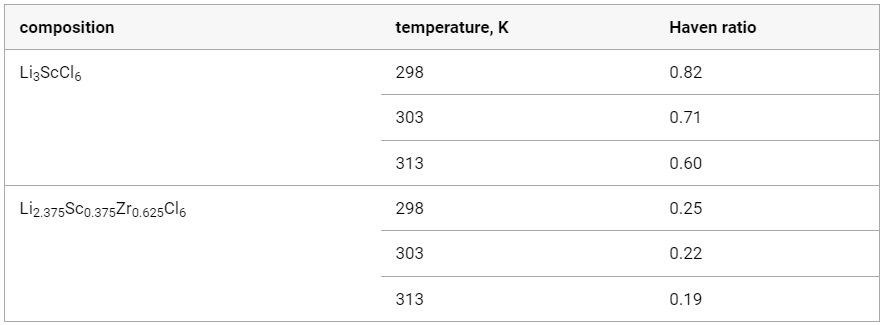
【表1】Li3ScCl6和Li2.375Sc0.375Zr0.625Cl6的避风比(HR)
还研究了三种代表性组合物Li3ScCl6、Li2.375Sc0.375Zr0.625Cl6和Li2.375Sc0.375Hf0.375Cl6的相稳定性和电化学稳定性。通过根据材料项目(MP)数据库中的竞争稳定相计算凸包(Ehull)上方的能量来计算相稳定性。原始和掺杂变体的Ehull值均低于25meV/原子(Li3ScCl6分别为21meV/原子,Li2.375Sc0.375Zr0.625Cl6为2meV/原子,Li2.375Sc0.375Hf0.625Cl6分别为14meV/原子),表明这些化合物在0K下是亚稳定相,并且可以通过熵效应在室温下稳定。使用基于MP数据库的既定方案计算了三种组合物的热力学本征电化学窗口。平衡电压曲线和相应的相平衡作为参考Li/Li+的外加电位的函数。Li3ScCl6及其掺杂变体均显示出宽电化学窗口,负极极限相同,均为4.25V,正极极限分别为0.91V、1.75V(M=Zr)和1.37V(M=Hf)。这些代表的热力学本征窗口比许多其他类别的SE宽得多,包括硫化物和氧化物SE(Li10GeP2S12(1.72−2.14V)、Li7P3S11(1.71−2.31V)、Li7La3Zr2O12(0.05−2.91V)和Li0.33La0.56TiO3.2(1.75−3.71V)。显示了Li3ScCl6及其Zr和Hf取代版本通过还原和氧化反应的分解能与锂化学势的函数关系。由于Li3ScCl6及其掺杂版本中的氧化过程主要发生在Cl−阴离子上,因此三种化合物显示出非常相似的氧化反应分解能。进行线性扫描伏安测试以验证这些化合物的电化学稳定性。Li3ScCl6、Li2.375Sc0.375Zr0.625Cl6和Li2.375Sc0.375Hf0.375Cl6的负极极限分别为4.28、4.26和4.22V,与计算结果非常一致。这些观察结果表明,Zr替代引起的变化可以忽略不计,而Hf替代则导致电解质的氧化电位略有降低。这些发现表明,与氧化电位较低的硫化物SE相比,氯化锂具有优异的抗氧化稳定性(例如,Li3PS4为2.31V,Li10GeP2S12为2.14V)。然而,Zr取代后,正极极限从0.97V(Li3ScCl6)增加到1.61V,Hf取代后增加到1.19V。这些值再次与计算非常吻合。尽管如此,掺杂变体的电化学窗口仍然落在常用正极材料的工作电压范围内,因此在组装成固态电池时不会导致降解。
通过制作采用Li2.375Sc0.375Zr0.625Cl6(缩写为LSZC)作为固态电解质层的ASSB,LiNi0.8Co0.1Mn0.1O2(此处标记为Ni80)或LiNi0.90Co0.05Mn0.05O2(标记为Ni90)作为正极(面载量高达6.11 mg·cm−2),Li−In合金作为负极,展示了掺杂SE的电化学性能。在LSZCSE层和Li−In负极之间放置一层薄薄的Li6PS5Cl,以防止氯化物SE还原(电池配置示意图见图5a)。电池在2.2−3.7V vs Li−In(2.8至4.3V vs Li/Li+)的电压范围内以不同速率充电和放电。图5b和图5c分别显示了Ni90和Ni80正极在30℃下不同倍率下的充放电容量。Ni90正极在0.1C下的初始充电容量为263.9 mAh g−1,放电容量为219.4 mAh g−1,初始库仑效率高达83.2%。将电流密度增加到0.5C倍率后,保留了200.7 mAh g−1的容量。电流密度的进一步增加证明了良好的倍率性能(1C时为178.6 mAh g−1),并且在返回到初始0.5C倍率后容量几乎完全恢复(图5b)。使用Ni80作为正极的ASSB也表现出良好的倍率性能,如图5c所示。通过在相同电压范围内对电池进行恒电流循环来研究相同全固态电池的寿命(图5d)。使用Ni90作为正极的电池在0.5C下循环超过200次后仍能保持约160.6 mAh g−1的容量(相当于78.1%的高保留率)。当与Ni80正极配对时,ASSB表现出更长的使用寿命;即,在1C下循环1000次后,容量保持率为82.7%。采用Li3ScCl6(此处和下文标记为LSC)作为固态电解质的ASSB也被组装作为比较。由于Li3ScCl6的离子电导率低得多,这些电池表现出比LSZC差的倍率性能,尽管在与Ni90或Ni80循环时与LSZC具有相当的容量保持率被观测到。然而,由于Zr取代后卤化物电解质的离子电导率增强,利用LSZC作为SE的ASSB在相同的电流密度下表现出显著增加的容量和更好的倍率性能。这些结果表明Zr取代的Li3ScCl6是一种很有前景的固态电解质材料,不仅具有高导电性,而且与正极材料相容。
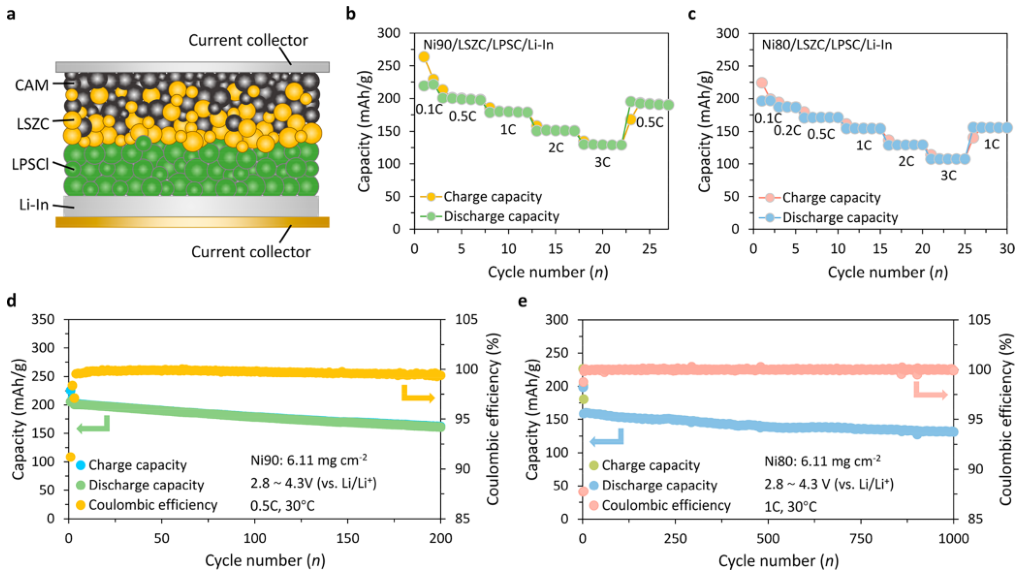
【图5】(a)Li−In/LPSC/LSZC/CAM固态电池示意图。(b)Ni90/LSZC/LPSC/Li−In固态电池在不同倍率(0.1C、0.5C、1C、2C和3C)下循环的倍率性能。(c)Ni80/LSZC/LPSC/Li−In固态电池在不同倍率(0.1C、0.2C、0.5C、1C、2C和3C)下循环的倍率性能。(d)Ni90/LSZC/LPSC/Li−In固态电池的循环性能。电池在前两个循环中以0.2C充电/放电,随后在其余测试中以0.5C充电/放电。(e)NCM80/LSZC/LPSC/Li−In固态电池的循环性能。电池在前两个循环中以0.1C充电/放电,随后在其余测试中以1C充电/放电。
在这项工作中,以Li3ScCl6作为原型,揭示了阳离子亚晶格无序和相关迁移对阳离子电导率的影响。当Zr取代Sc位点时,沿c轴的Li+离子传输通道变宽,相应的迁移能垒降低。因此,室温离子电导率提高至2.2 mS cm−1。AIMD分析和NMRPFG测量相结合表明,Li2.375Sc0.375Zr0.625Cl6离子电导率的显著增强归因于调整Li+/空位浓度引起的Li+离子相关迁移比率的提高。优异的离子传导性能以及高氧化电位有助于固态电池良好的循环和倍率性能。工作强调了调节Li+/空位比作为调节相关迁移从而提高阳离子电导率的一种手段的功效。这些发现为无机框架中快离子传导的起源提供了新的见解,并且可以作为固态电解质设计的补充指南。
参考文献
Superionic Conductivity Invoked by Enhanced Correlation Migration in Lithium Halides Solid Electrolytes
R. Li, P. Lu, X. Liang, L. Liu, M. Avdeev, Z. Deng, S. Li, K. Xu, J. Feng, R. Si, F. Wu*, Z. Zhang*, Y. Hu*
ACS Energy Letters (IF=22) 2024, 9, 1043–1052
https://doi.org/10.1021/acsenergylett.3c02496